截至 2022 年 5 月 5 日,由 SARS-CoV-2 引发的全球 COVID-19 冠状病毒确诊病例已累计达到 515,354,713 例,累计死亡人数达 6,269,587 例。其中,美国、印度、巴西仍是感染病例总数最多的 3 个国家。新冠疫情的流行在卫生安全、国际交流、社会、经济等方面对全球产生了重大影响。在上期文章中,我们概述了当前应用人类多能干细胞衍生的类器官和成体类器官来研究 SARS-CoV-2 趋向性、宿主反应和免疫细胞介导的宿主损伤,以及进行药物发现和疫苗开发的努力。在此,总结了基于类器官的 COVID-19 研究中使用的技术,讨论了目前面临的挑战,并提供了应用类器官模型研究 SARS-CoV-2 和未来新兴病毒的前景。
在基于类器官的 COVID-19 研究中,hPSC 衍生的类器官和成体类器官都被使用,二者在可用性、可编辑性、成熟度和多样性方面各有利弊。理论上,hPSCs 具有无限的增殖能力和发育潜力,可以在所有三个胚层中产生类器官(下图)。hPSC 衍生的类器官可以轻松扩大规模,从而允许进行大规模研究,例如代谢分析和药物筛选。并且一些类器官,如大脑和心脏类器官,只能从 hPSC 获得。相比之下,来自成人组织的成体类器官在很长一段时间内自我更新能力有限,这限制了它们在大规模研究中的应用。才外,与成体类器官相比,基因敲除和精确的基因编辑技术在 hPSCs 中得到了更好的建立,这使得探索单一变体在病毒感染中的生物学功能成为可能。成体类器官的一大优势是成熟度,不像大多数 hPSC 衍生的类器官需要做更多的工作来进一步改善成熟状态。并且,成人类器官可以很容易地从不同背景的捐赠者处获得,用于探索遗传背景对疾病发展的影响。
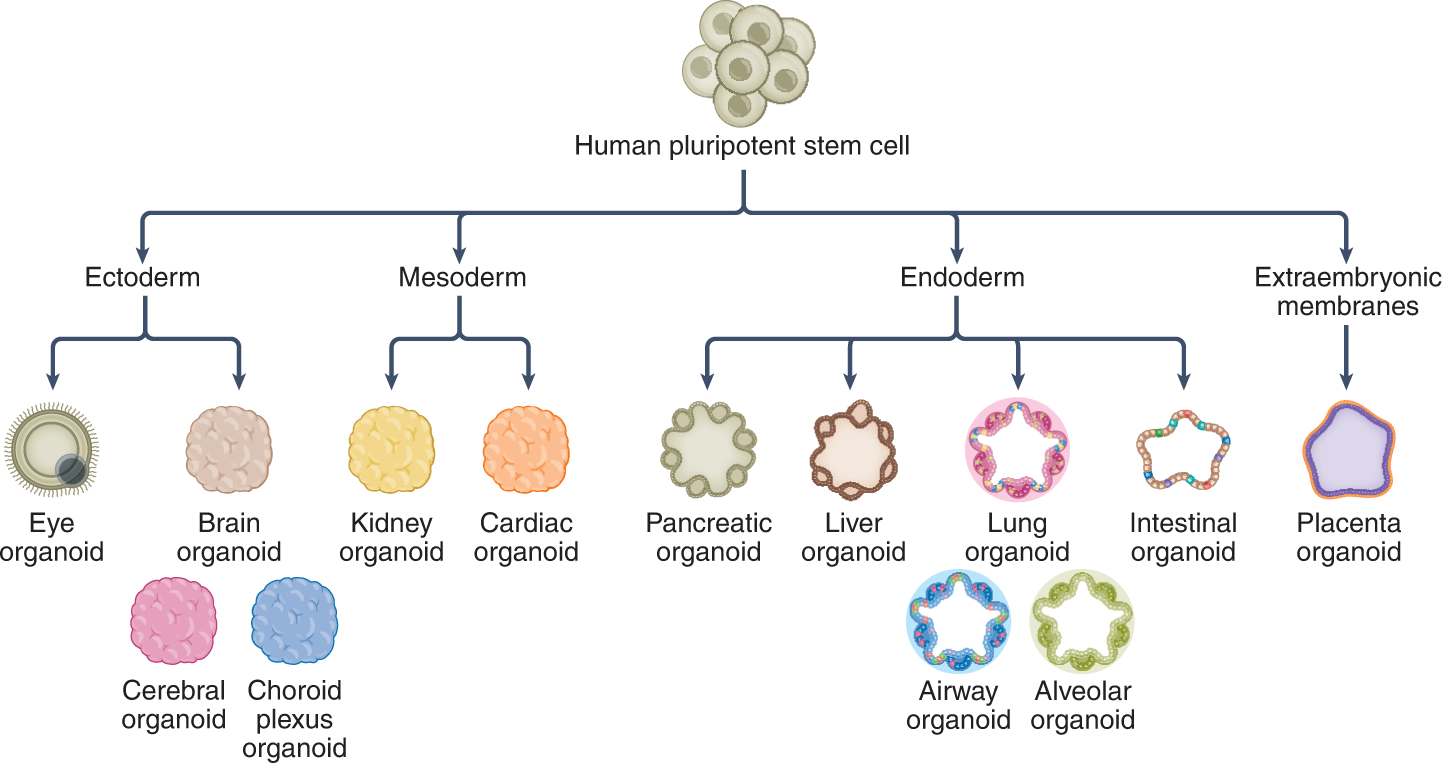 hPSC 在三个胚层中定向分化为类器官。
hPSC 在三个胚层中定向分化为类器官。
在过去两年中,将类器官应用于 COVID-19 疾病建模取得了重要进展。然而,为了进一步优化感染性疾病的类器官模型,还应该进行更多的研究,如通过增加利基/免疫细胞来提高类器官的复杂性,结合 3D 打印和器官芯片技术来开发与人类系统的生理和病理密切相关的平台,应用单细胞技术来进行高分辨率的病毒-宿主相互作用的深入研究,以及应用基因组测序和基因编辑来探索病毒感染期间的基因型-表型相关性(下图)等等。这些技术将增强类器官培养方法并加速新的抗病毒疗法和疫苗的研究进程,有助于在未来研究其他新病毒。
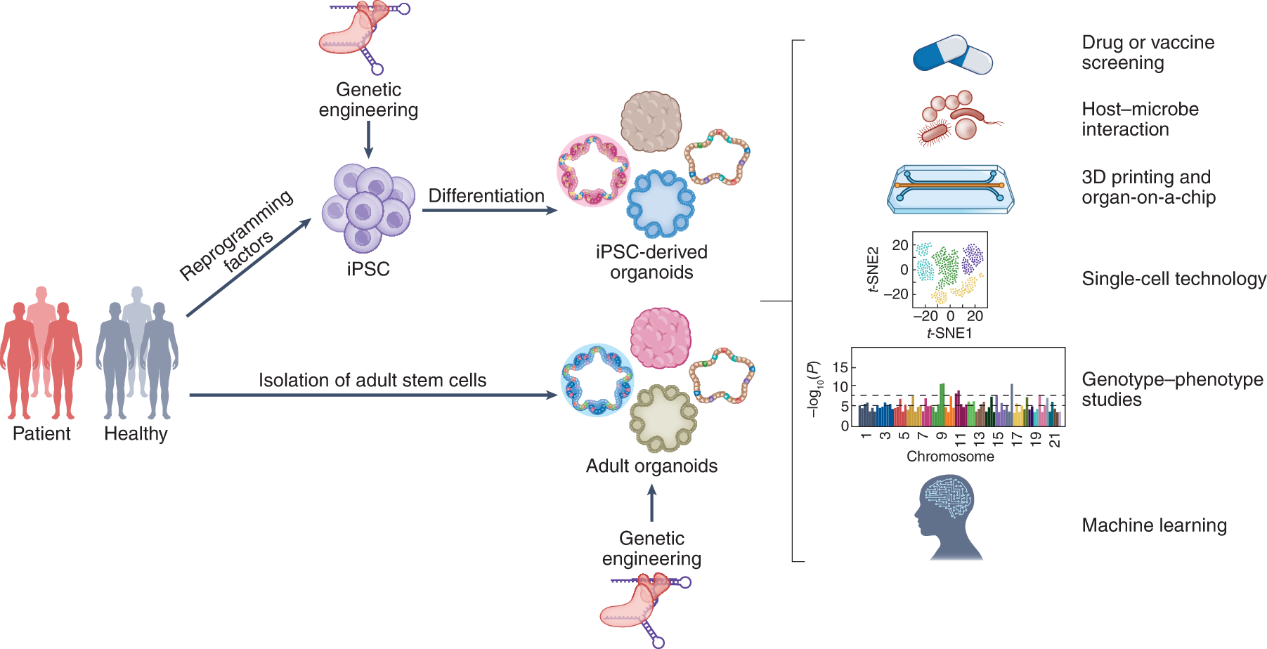 类器官模型在传染病研究中的未来应用。
类器官模型在传染病研究中的未来应用。
大多数用于 COVID-19 研究的类器官平台只包含宿主组织/器官的细胞,其中缺乏其他利基成分,如免疫细胞和血管系统的细胞。然而,免疫细胞是 COVID-19 病理生理学和疾病进展等许多方面的关键。与直接感染相比,免疫介导的损伤可能发挥同等甚至更重要的作用。因此,有免疫细胞的体外共培养器官可用于研究由免疫细胞引起的 COVID-19 的病理生理学,以及直接感染的后果。此外,有免疫细胞的器官可以更好地了解受感染的宿主细胞和免疫细胞之间的相互作用,受感染细胞释放的免疫调节分子如何影响免疫成分,以及免疫反应如何反过来影响受感染的宿主组织。
最近,一个包含 hPSC 衍生的心肌细胞和巨噬细胞的免疫宿主共培养系统表明,在 SARS-CoV-2 感染后,hPSC 衍生的心肌细胞会分泌 CC 基序趋化因子配体 2(CCL2),这是一种募集单核细胞的趋化因子。单核细胞分化成巨噬细胞,通过分泌促炎细胞因子 TNF 和 IL-6 来损害心脏组织。此外,使用免疫宿主共培养系统进行的高含量化学筛选确定了一种 janus 激酶抑制剂,可阻断巨噬细胞介导的心脏细胞损伤。巧合的是,一种 janus 激酶抑制剂 baricitinib 已获得 FDA 的紧急使用授权,用于治疗 COVID-19 住院患者。总之,这些例子共同强调了基于类器官的模型中免疫成分对研究病毒感染的重要性。
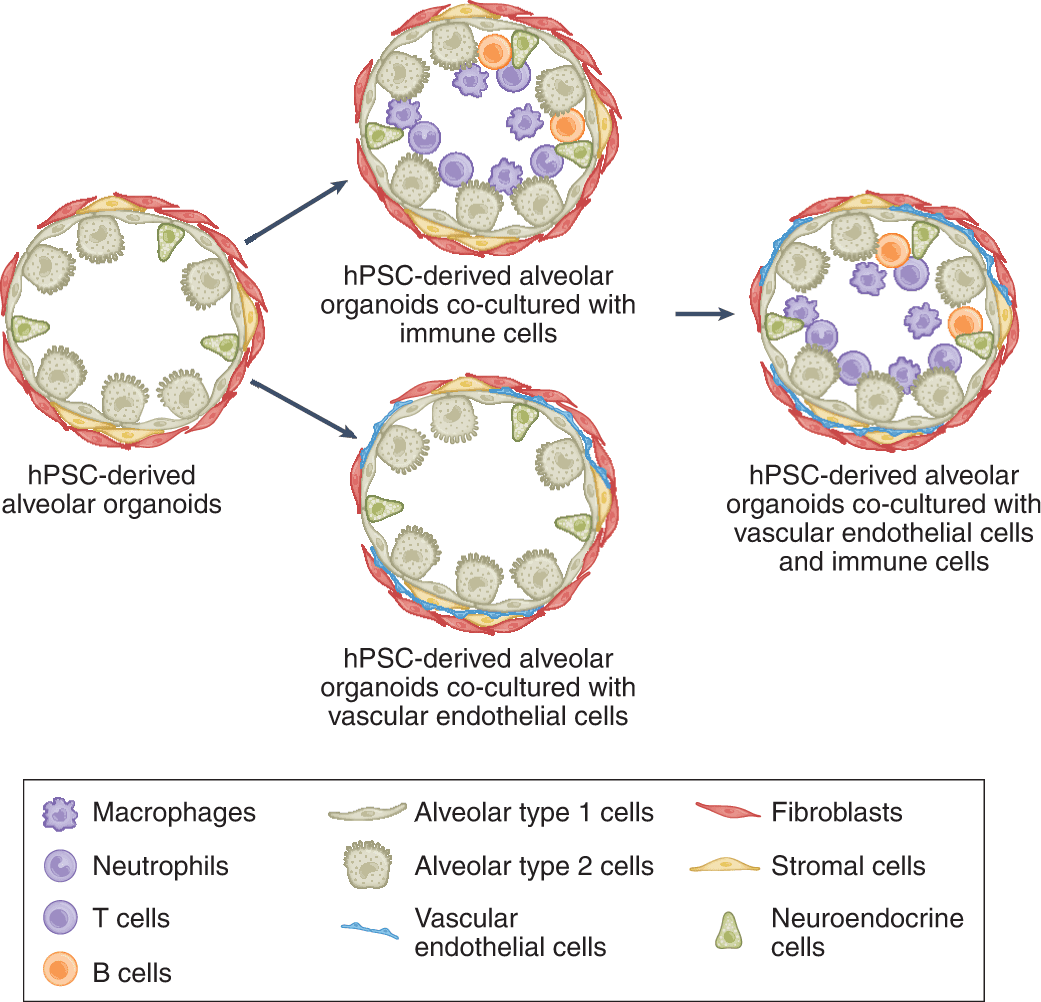
血管-免疫-肺泡类器官的发育。
许多类器官平台的另一个限制是缺乏血管。血栓并发症在 COVID-19 中很常见,并导致死亡和发病。将类器官与血管内皮细胞和周细胞共培养,以在合适的空间结构中形成含有血管的类器官,为进一步开发类器官模型系统提供了希望。包含宿主类器官、免疫细胞和血管细胞的免疫-血管-类器官模型,将推进类器官技术的发展,并为研究新出现的病毒提供下一代模型(上图)。
除了在类器官中包含不同的细胞类型外,创建具有适当细胞空间位置和器官间相互作用的类器官也很重要。3D 生物打印技术使用载有组织特异性细胞类型的生物墨水,通过分层打印技术重建人体器官样结构。3D 生物打印产生的器官模拟系统技术在研究人类病毒感染方面具有广阔的前景。例如,3D 生物打印的肺样结构可用于研究 SARS-CoV-2 感染,因为它们在由多层和细胞类型组成的复杂中空结构中提供了空气-细胞界面,这是传统组织工程方法无法实现的。

另一项与类器官相结合的创新技术是器官芯片,它是用于在连续灌注的小室中培养细胞和组织的微流体装置。器官芯片系统允许创建动态和可控的微环境,适用于研究病毒与宿主的相互作用、病毒治疗耐药性的演变、新抗病毒疗法的开发和潜在的病毒发病机制。使用血管化的肺芯片模型研究 SARS-CoV-2 感染,肺泡上皮细胞表现出对感染的易感性和血小板内皮细胞粘附分子(PECAM-1)的表达降低,导致促凝微环境的建立和屏障的破坏。在芯片上培养的类器官为重现器官水平的生理功能提供了新的可能性,这将进一步加深对 COVID-19 发病机制的理解。

类器官的一个主要优点是它们包含多种类型的细胞,可以利用这些细胞来探索病毒与不同宿主细胞之间的相互作用,以及病毒感染后宿主细胞之间的相互作用。在 COVID-19 研究的早期阶段,scRNA-seq 被广泛应用于确定 SARS-CoV-2 进入因子在类器官内不同类型细胞中的表达。然而,基于 scRNA-seq 分析的总 ACE2 表达较低。例如,肺 AT2 细胞中 ACE2+ 细胞的百分比在 0.3% 和 2.4% 之间变化,这反映了 scRNA-seq 平台的检测灵敏度较低。因此,非常需要仔细解释 SARS-CoV-2 进入因子表达的 scRNA-seq 数据。scRNA-seq 数据需要通过独立的方法进一步验证,如免疫染色或流式细胞分析。尽管在技术上具有挑战性,但 scRNA-seq 开始被应用于在 BSL-3 环境中直接分析 SARS-CoV-2 感染的组织/类器官。这些类型的研究有望在单细胞分辨率下深入了解 SARS-CoV-2 感染后的宿主细胞反应和宿主细胞相互作用。
hPSC 和成体类器官都可以来自具有不同遗传背景的个体,这为探索遗传变异对疾病进展(包括病毒感染)的影响提供了有用的模型。一方面,基于 CRISPR 的基因编辑方法可以有效地敲除单个基因/位点或敲入单个变体,为生成等基因 hPSC/类器官提供了高通量平台。这些等基因 hPSC/类器官可用于确定单个基因/基因座,甚至单核苷酸多态性在病毒感染和宿主损伤中的确切作用。另一方面,通过将全基因组测序和来自不同供体的类器官筛选相结合,科学家可以进行基因型-表型研究,以确定与病毒感染相关的新基因/位点/变异。也可以使用由基因编辑工具开发的等基因类器官模型进一步验证已识别的基因/位点/变体。此外,这些来自不同供体的 hPSC/类器官也可用于研究个体对抗病毒药物的反应,这将有助于开发针对 COVID-19 的个性化治疗。

目前,深度机器学习已在分子和细胞生物学、药物发现、蛋白质结构预测和转化生物医学中得到有效应用。深度机器学习在病毒遗传学领域的应用主要集中在预测与耐药性相关的病毒突变。DeepNEU 是一种基于全连接递归神经网络架构的无监督深度机器学习技术,每个输入都有一个网络处理层,它使用一组定义的重编程转录因子来模拟 iPSC 系统。在 DeepNEU 中,可以模拟 AT2 细胞,并显示能够模拟 SARS-CoV-2 病毒感染。受感染的肺细胞和类器官可用于刺激和评估 SARS-CoV-2 基因组中潜在功能突变的影响。这些数据与最近公布的数据一致,为确定潜在有效的抗 SARS-CoV-2 药物组合提供了一种新的方法。

使用类器官平台的研究对 COVID-19 疾病建模和药物发现做出了重大贡献。与动物模型相比,由于缺乏血管系统、免疫细胞和器官间通讯,类器官平台仍然存在一些局限性。现阶段,疫苗和药物开发仍需要用到动物模型。未来,这些类器官平台将用于模拟更复杂的器官,模拟器官内相互作用,探索致病机制。来自健康或 COVID-19 供体的多种组织和类器官可以为不同年龄、性别或种族群体的个体的病毒易感性提供可靠的分子评估,并为当前和未来的流行病提供个性化的治疗策略。
原文链接:https://www.nature.com/articles/s41592-022-01453-y
作为全球优质的临床前药物开发服务供应商,安必奇生物拥有丰富的体外模型构建、器官芯片开发等代理经验。提供优质、完善的器官芯片设计及开发服务,以帮助客户获取高仿、节能的生理学研究及药物开发工具。目前已建立能够模拟心脏、肝脏、肺、肾、脑、肠等器官的微结构和功能的芯片模型。可从材料、制备技术、仪器、以及商业化等方面实现个性化定制。欢迎免费咨询!
24小时服务在线

