体外转录 mRNA 合成方面的进展激发了对基于 mRNA 的基因疗法的大量研究,包括下一代疫苗的开发。与质粒 DNA 相比,mRNA 提供了更安全和更可控的基因表达,因为其几乎消除了整合到宿主基因组中的风险。此外,mRNA 递送还可以在对 DNA 转染基本不敏感的细胞群中实现更有效的表达,如T细胞。然而,由于 mRNA 分子的大小和亲水性,它们是不透膜的,这使得安全和有效的细胞膜 mRNA 递送成为其临床应用的主要障碍。

非病毒纳米颗粒(Nonviral nanoparticle, NP)制剂已成为有前途的 mRNA 递送载体。为了充分实现 mRNA 疗法的效用,必须设计合理的 NP 系统以克服细胞内障碍,例如细胞内化和逃离内体隔离。其中,测量 NP 在关键递送瓶颈的性能够改进 NP 设计,突出了对高通量和高内涵体外定量测定的需求。现存的几种测定方法均存在一定的缺陷,如LysoTracker 染料法仅提供间接评估,无法体现有效的内体逃逸或破坏;而透射电子显微镜(TEM)成像法虽然可以确认内体破坏和逃逸,但却无法进行高通量分析,不能在活细胞上进行,并且需要电子密集标记,可能会改变原生 NP 系统的特性。因此,急需开发具有高预测能力的定量、高通量筛选平台。
2022 年 1 月 5 日,美国约翰霍普金斯大学医学院的研究人员在 SCIENCE ADVANCES 杂志上发表了题为“高通量和高内涵的生物测定能够调整聚酯纳米颗粒的细胞摄取、内体逃逸和 mRNA 的的系统性体内递送”的研究论文。该研究使用基于图像的高通量和高内涵筛选开发了一种纳米颗粒摄取和内体破坏的双重检测方法。使用基因编码的 Galectin 8 荧光融合蛋白传感器,可以通过该传感器在受损内体膜上的聚集来检测内体破坏。同时,使用荧光标记的 mRNA 对核酸内吞作用进行了量化。利用生物可降解颗粒对 mRNA 进行有效的非病毒性系统递送,为遗传医学和人类健康研究开辟了新的途径。

该研究使用工程化 B16-F10 鼠黑色素瘤细胞对 Gal8-mRuby 内体破坏传感器进行基因编码,以促进 NP 摄取和内体破坏的同步表征。通过量化携带 Cy5 标记的核酸的 NPs 在细胞内的递送所产生的 Cy5 点来测量NP的摄取;通过量化 Gal8-mRuby 在受损的内体膜上聚集所产生的 mRuby 点来测量内体破坏(图 1A)。使用 CellInsight CX7 LZR 高内涵成像仪以 20 倍放大率捕获 96 孔板的每孔 20 个视野,以高通量方式进行 NP 摄取和内体破坏的双重检测。然后优化图像分析算法,并通过推断染色的细胞核周围的细胞体来识别细胞,并提供每个细胞的点状计数(图 1B)。平均而言,每个 NP 制剂收集了超过 15,000 个细胞的细胞内点状计数。
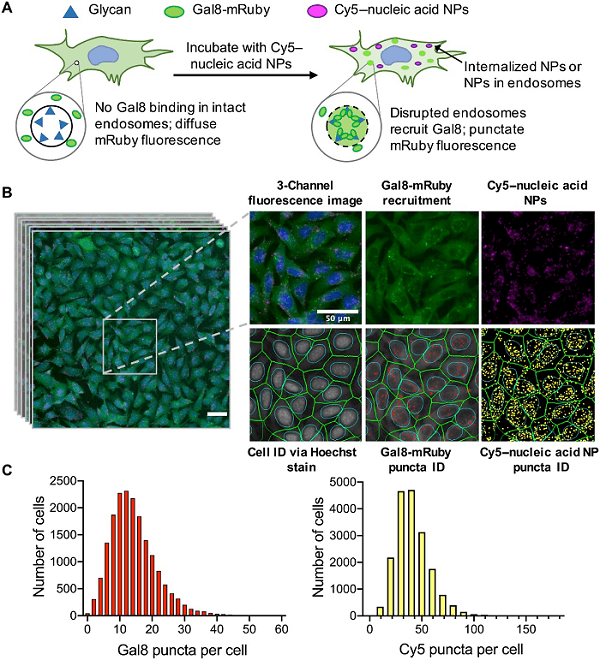 图1. 基于图像的 NP 摄取分析和 GAL8 内体破坏测定。
图1. 基于图像的 NP 摄取分析和 GAL8 内体破坏测定。
该研究合成了两个系列的具有不同疏水单体含量的可生物降解聚(β-氨基酯)(poly(beta-amino ester)s, PBAE)聚合物,以研究聚合物骨架疏水性对 NP 摄取、内体破坏和转染能力的影响。这些聚合物首先被合成为亲脂性 PBAE 三元共聚物,由线性二丙烯酸酯(B7)与亲水胺(S90)和通过 Michael 加成反应合成的疏水胺(ScX)组成(图2)。在一个系列中,聚合物的疏水性是通过加入 30 摩尔百分比的不同脂质尾长的疏水胺来改变的;在第二个系列中,是通过改变 Sc12 单体的摩尔含量来改变的。然后用单体 E63 对两个系列中的聚合物进行封端以形成 PBAE 四元共聚物,分子量在 4 到 10 kDa 的范围内。在水性缓冲液中进行简单的混合后,发现所有聚合物都能快速自组装成带有质粒 DNA、mRNA 和 siRNA 的 NPs。包裹核酸货物的 NPs 直径为 100 至 400 nm。
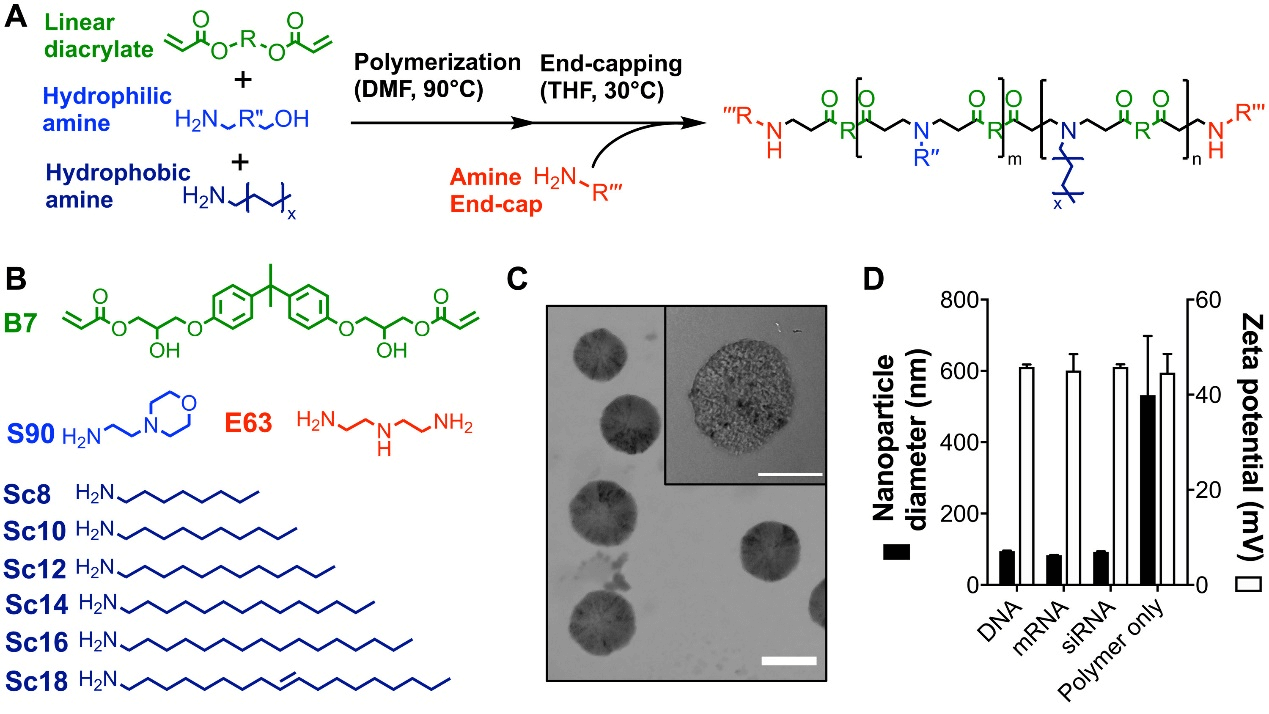 图2. PBAE NPS的化学结构和表征。
图2. PBAE NPS的化学结构和表征。
接下来评估了 NP 的摄取、内体破坏和基因递送的效果。siRNA NPs 的转染是通过 siRNA 介导的绿色荧光蛋白(GFP)在GFP+ 的细胞中被敲低来评估的,而 DNA 和 mRNA NPs 的转染是通过在非 GFP+ 细胞中编码 GFP 基因的 DNA 或 mRNA 的功能性递送所产生的 GFP 表达来评估的。所有 PBAE NP 制剂均保持 >90% 的细胞活力。在两个 PBAE 聚合物系列中,增加聚合物主链疏水性通常会增加核酸摄取和转染(图 3A)。Gal8 内体破坏情况正好相反,与含有 0% Sc12(疏水性最低)的聚合物相比,含有 100% Sc12(疏水性最强)的聚合物导致 Gal8-mRuby 点状物计数减少一半。在测试的五种市售材料中,Lipofectamine 3000 在所有核酸类型中的转染率最高,其次是 25-kDa 支链 PEI。这些市售材料的转染与内体破坏呈正相关,并且未观察到与 NP 摄取的显著相关性。即使转染效果相似,这些材料的 Gal8 点状计数也远低于 PBAE NPs 所达到的计数,这表明这两类材料使用不同的机制来实现内体破坏。
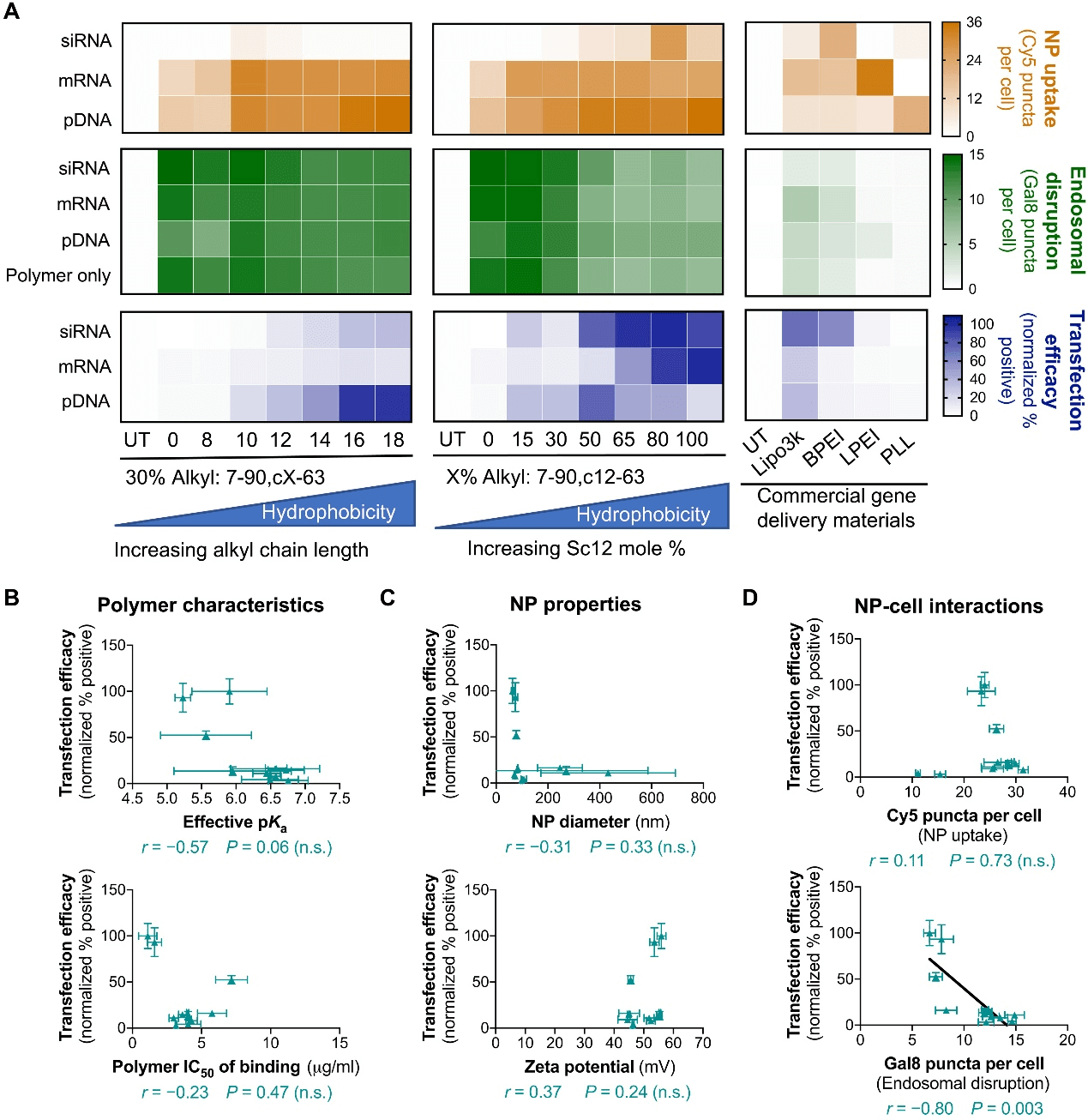 图3. 验证PBAE NPs和商业试剂对 B16-F10 细胞递送不同核酸载体的双重 NP 吸收/Gal8 内体破坏试验。
图3. 验证PBAE NPs和商业试剂对 B16-F10 细胞递送不同核酸载体的双重 NP 吸收/Gal8 内体破坏试验。
接着,进一步评估了各种聚合物和 NP 特性对转染效果的预测能力。聚合物与核酸结合的中位抑制浓度(IC50),数值越大表明核酸结合亲和力越弱,与 DNA 转染呈负相关,但与 siRNA 敲低呈正相关。这可能是由于每种核酸在细胞内的作用位点不同。在这些实验中未观察到 mRNA 转染与核酸结合亲和力显著相关(图 3B)。NP 大小和 Zeta 电位的标准生物物理特性测量显示与转染效率没有明显关联(图 3C)。该研究提出的的基于高通量和高内涵成像的检测方法量化的 NP-细胞相互作用显示,PBAE 转染通常与 NP 的摄取正相关,与 Gal8 内体破坏负相关(图3D)。
研究人员接下来通过合成端基变异聚合物系列研究了聚合物端基结构对 NP 摄取和内体破坏的影响。这是通过使用中等疏水性的 PBAE 三元共聚物骨架(7-90,c12-X,50%-Sc12),再将 11 种不同的端基单体分别单独与其偶联来完成的(图 4A)。为了检验该双重测定可用于进一步确定聚合物端基结构如何影响不同细胞类型中 NP 功能,并进一步评估新的高通量和高内涵生物测定的稳健性,研究人员在三种不同类型的细胞上评估了这些聚合物:B16-F10 鼠黑色素瘤细胞,RAW 264.7 鼠巨噬细胞和 NIH/3T3 鼠成纤维细胞。结果显示 B16-F10 细胞中的 mRNA 转染水平最高,RAW 264.7 巨噬细胞的转染水平中等,而 NIH/3T3 成纤维细胞的转染水平最低(图 4A)。内体破坏与 RAW 和 3T3 细胞的 mRNA 转染水平呈正相关,但与 B16 细胞无关,当三个细胞系一起评估时,具有显著的正相关(图 4B)。在 NIH/3T3 细胞中观察到最高的 NP 摄取水平,这表明 mRNA 转染水平最低,并且一般来说,mRNA 转染与这些细胞类型中的 PBAE NP 摄取没有显示出显著相关性(图 4C)。总之,这些结果表明,对于具有相同聚合物骨架(和类似的疏水性)的 PBAEs,端基结构在内体破坏中起着重要作用。此外,对于这些 PBAEs,内体破坏,而不是 NP 摄取,正在成为有效 mRNA 递送的更大瓶颈。
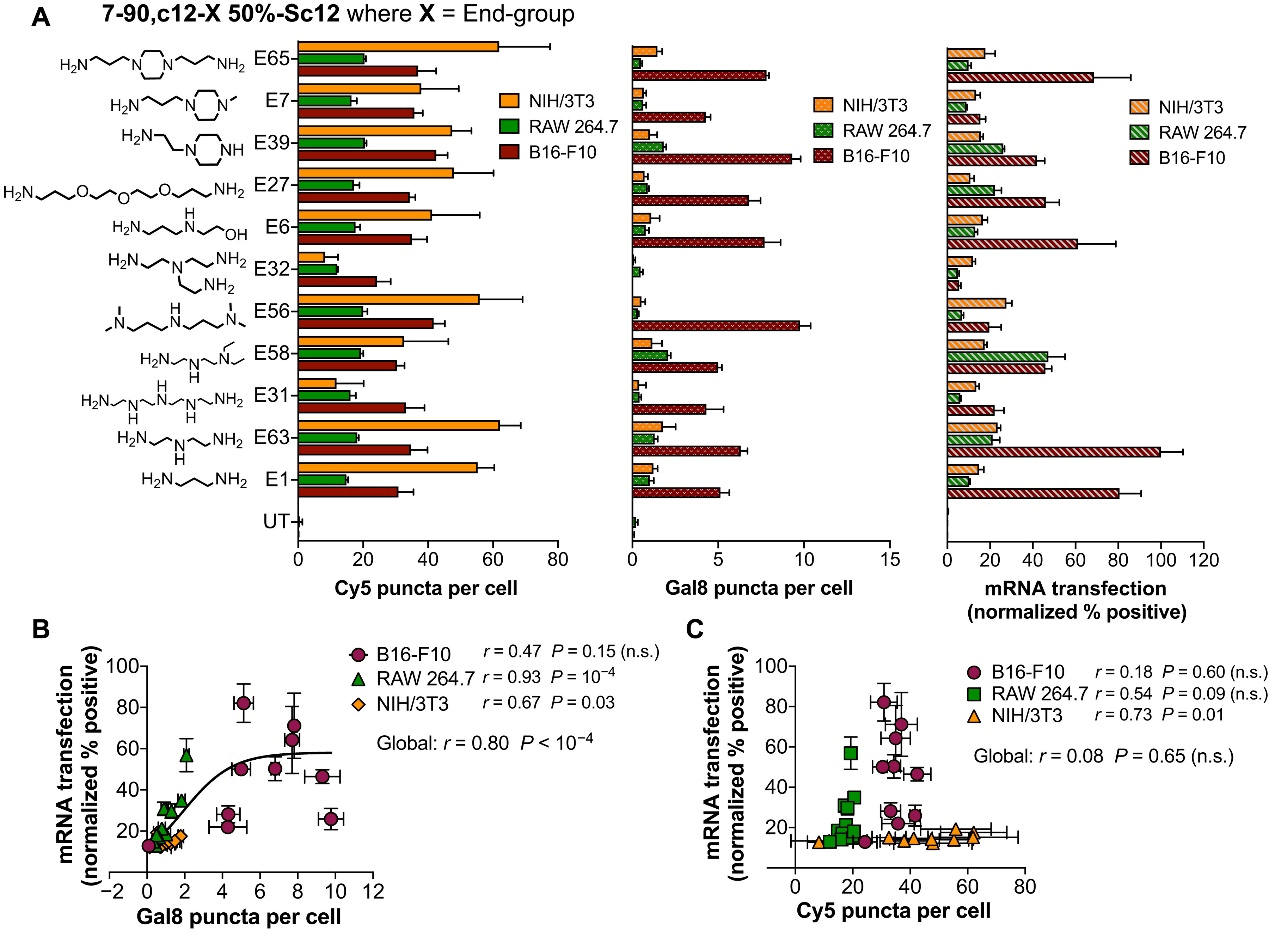 图4. 聚合物端基结构对多个细胞系的mRNA转染效力的影响。
图4. 聚合物端基结构对多个细胞系的mRNA转染效力的影响。
接下来研究人员对小鼠静脉注射封装有编码萤火虫荧光素酶(firefly luciferase, fLuc)的 mRNA 的 NPs,来对 NPs 的体内 mRNA 递送能力进行了表征。在体内实验中,用 PEG-lipid DMG-PEG2k (1,2-dimyristoyl-rac-glycero-3-methoxypolyethylene glycol-2000)配制 NPs,并在磷酸盐缓冲盐水(PBS)中透析(称为 PBAE + PEG-lipid NPs;图 5A)。先前的研究表明,在递送 siRNA 的脂质 NPs 中,含有大于 14 个碳烷基链的 PEG 脂质会抑制肝脏 siRNA 的递送,因为脂质从 NPs 中解吸不充分。因此,该研究中使用了 DMG-PEG2k(含有 14 个碳烷基链)。据观察,将 DMG-PEG2k 掺入 PBAE 四聚物中可减小 NP 尺寸并中和表面电荷。尽管减少了 NP 摄取和内体破坏,但 PEG-lipid 涂层在体外并未显著改变转染效果。在体内给药时,与没有 PEG 包裹的 NPs 相比,PEG 包裹和透析的 NPs 能够显著提高 mRNA 表达。
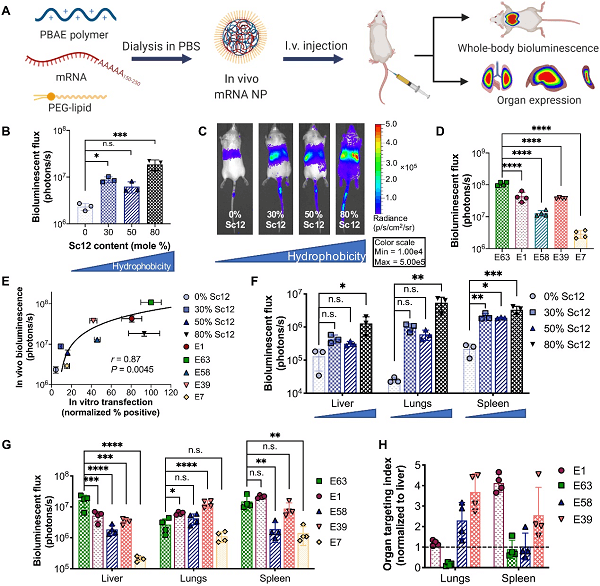 图5. PEG 包裹的 PBAE NPs 递送 mRNA 的体内验证。
图5. PEG 包裹的 PBAE NPs 递送 mRNA 的体内验证。
选择聚合物骨架中 Sc12 含量为 0 至 80% 的四种聚合物和五种具有不同聚合物端基的聚合物来评估聚合物骨架和端基结构对体内表达的影响。在全身水平上,骨架疏水性增加通常会导致 mRNA 表达增加(图 5B 和 5C),而聚合物端基变异导致不同的体内表达水平(图 5D)。总体而言,体内表达与 B16-F10 细胞的体外转染呈正相关(图 5E),但与 NP 的吸收或内体破坏没有明显的相关性,表明体外筛选对这些纳米材料的体内性能的预测能力有限。在单个器官的水平上,增加骨架的疏水性增加了在所有被评估的器官中的表达(图 5F),而聚合物端基在将 NP 表达靶向特定器官中发挥了主要作用(图 5G)。当肺部和脾脏中的表达与肝脏中的表达归一化时,聚合物 E1 在脾脏中优先表达,聚合物 E63 在肝脏中优先表达,聚合物 E58 在肺部优先表达,而聚合物 E39 在肺部和脾脏中几乎平均分配(图 5H)。
该研究使用 Ai9 小鼠模型进一步探测了在每个器官中转染的细胞群,该模型在 tdTomato 报告基因上游包含一个动态表达终止盒。通过尾静脉注射将包裹 Cre mRNA 的 NPs 注射到 Ai9 小鼠中,转染的细胞进行 Cre-Lox 重组,导致 tdTomato 表达,在注射后 3 天通过流式细胞测量(图 6A)。结果发现,系统性给药的 7-90,c12-63,80%-Sc12 NPs 转染了近 0.2% 的脾脏细胞、2% 的肝脏细胞和 4% 的肺细胞,并且在评估的其他器官中的转染水平极低(图 6B)。全身注射后,肺部超过 20% 的内皮细胞被转染,与之前关于相关 PBAE 结构的报道一致,还有大量巨噬细胞和树突状细胞(图 6C)。内皮细胞也占了肝脏(33%)和脾脏(23%)中转染细胞的很大一部分(图 6D)。
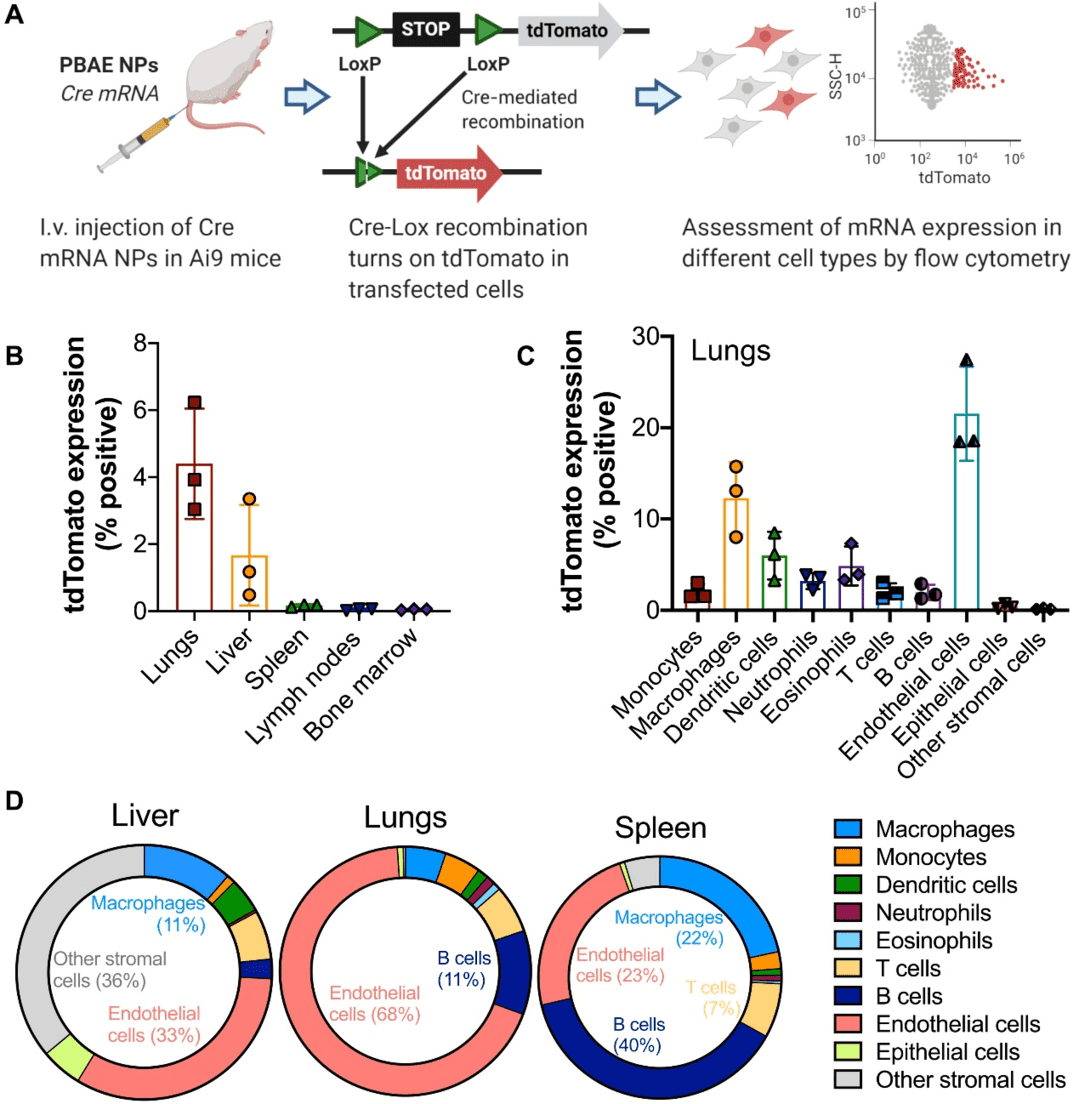 图6. 在不同类型的细胞中评估体内 mRNA 转染。
图6. 在不同类型的细胞中评估体内 mRNA 转染。
为扩大 mRNA 疗法的治疗潜力,需要一个高通量、标准化的 NP 筛选平台,该平台应当能够定量评估细胞内递送步骤,并对转染效果有很强的预测能力。在这项研究中,研究人员开发了一个高通量、高内涵、基于成像的筛选平台,旨在同时评估核酸递送 NPs 的细胞内化和内体破坏能力,只需要宽视场、落射荧光显微镜就能全面评估胞质隔室。使用两个系列的 PBAE 四元聚合物来验证该筛选平台,结果表明必须达到内体破坏的阈值,才能使基因递送有效地发生。总的来说,该研究数据表明,内体逃逸是 mRNA 递送到难以转染细胞的主要障碍,并且由聚合物端基介导的差异基因递送功效主要是由于它们促进内体破坏的能力。未来,PBAE NP 制剂的先天性器官趋向性也许可以与其他技术相结合,以增强选择性器官靶向性和潜在的细胞类型特异性靶向性。随着进一步的研究,这种基于 PBAE 的材料可能有望临床用于 mRNA 递送以促进人类健康。
原文链接:
https://www.science.org/doi/10.1126/sciadv.abk2855
安必奇生物致力于为国内外客户提供 MicroRNA Agomir/ Antagomir 递送系统研究和分析相关服务。代理技术团队拥有多年的运载体定制经验,能在较短的时间内为客户提供理想的载体筛选和制备服务。另外,还完善了一整套 miRNA 的合成及纯化技术,能够提供优质的 miRNA 合成产品,促进客户相关项目的快速进展。欢迎免费咨询!
24小时服务在线

