肾脏属于泌尿系统的一部分,负责过滤血液中的杂质、维持体液和电解质的平衡,最后产生尿液经由后续管道排出体外,在从体内消除外源性物质及其代谢物方面起着关键作用,影响药物疗效和安全性。阿片类药物过量、依赖和成瘾是主要的公共卫生危机之一。慢性肾病(chronic kidney disease, CKD)患者阿片类药物过量的风险很高,因此提供能够准确预测阿片类药物在 CKD 患者中肾脏清除率(renal clearance, CLr)和药物生理学的模型至关重要,可以促进治疗方案的优化。
肾脏排泄是通过肾小球滤过、转运蛋白介导的主动分泌和被动重吸收的协同作用实现的。因此,要在体外评估肾脏药物排泄,模型必须结合转运蛋白介导的主动分泌和跨肾小管上皮的被动渗透过程。目前已经提出的几种预测药物肾脏分泌活性方法,包括肾脏切片、使用转染细胞的体外-体内推断法(in vitro–in vivo extrapolation, IVIVE),以及二维 Transwell 中的 PTEC 单层等。然而,这些方法都具有一定的局限性,限制了它们的效用。例如,由于近端肾小管切口的闭塞,肾脏切片无法评估药物在近端肾小管腔内的净分泌量。IVIVE 方法通常假定肾小管的分泌仅由 OAT 介导的转运决定,而未考虑其他可能对净分泌有贡献的未知转运体等等。因此,能够将拟态流动和剪切应力相结合,作为改进系统的器官芯片技术越来越受到科研人员的关注。
2021 年 11 月 1 日,华盛顿大学药学院的研究团队在 Scientific Reports 杂志上发表了题为“通过模拟阿片类药物在肾脏近端小管微生理系统中的处置,弥合计算机模型与体内的差距”的研究论文。该研究使用血管化的人近端小管微生理系统结合母体-代谢物全身生理药代动力学(PBPK)模型,预测 CKD 患者中吗啡及其活性代谢物吗啡-6-葡萄糖醛酸(M6G)的肾脏清除率和全身性处置情况。结果表明,该系统成功预测了健康人和 CKD 患者的 CLr 和血浆浓度-时间曲线。微生理系统与数学模型一起成功预测了 CKD 患者和健康受试者的阿片类药物的肾脏清除率和全身性处置。

血管化人近端小管微生理系统(VPT-MPS)的构造如下图所示,用于评估吗啡和 M6G 的肾小管分泌。完整的双通道装置由内皮血管、间质基质和上皮小管组成,允许评估药物进入和从内皮血管外渗的顺序过程,在间质基质上的扩散以及溶质在小管上皮的协调吸收和流出。内皮细胞和上皮小管细胞,人脐静脉内皮细胞(HUVECs)和人原发性近端肾小管上皮细胞(PTECs)分别被种在 MPS 装置的并排通道中,在流动条件下培养,并用于运输实验。VPT-MPS 中 PTECs 的免疫细胞化学染色显示了有机阴离子转运体(organic anion transporter, OAT)1 和 3 以及定位在基底外侧膜的有机阳离子转运体(organic cation transporter, OCT)2 的表达(图1c)。
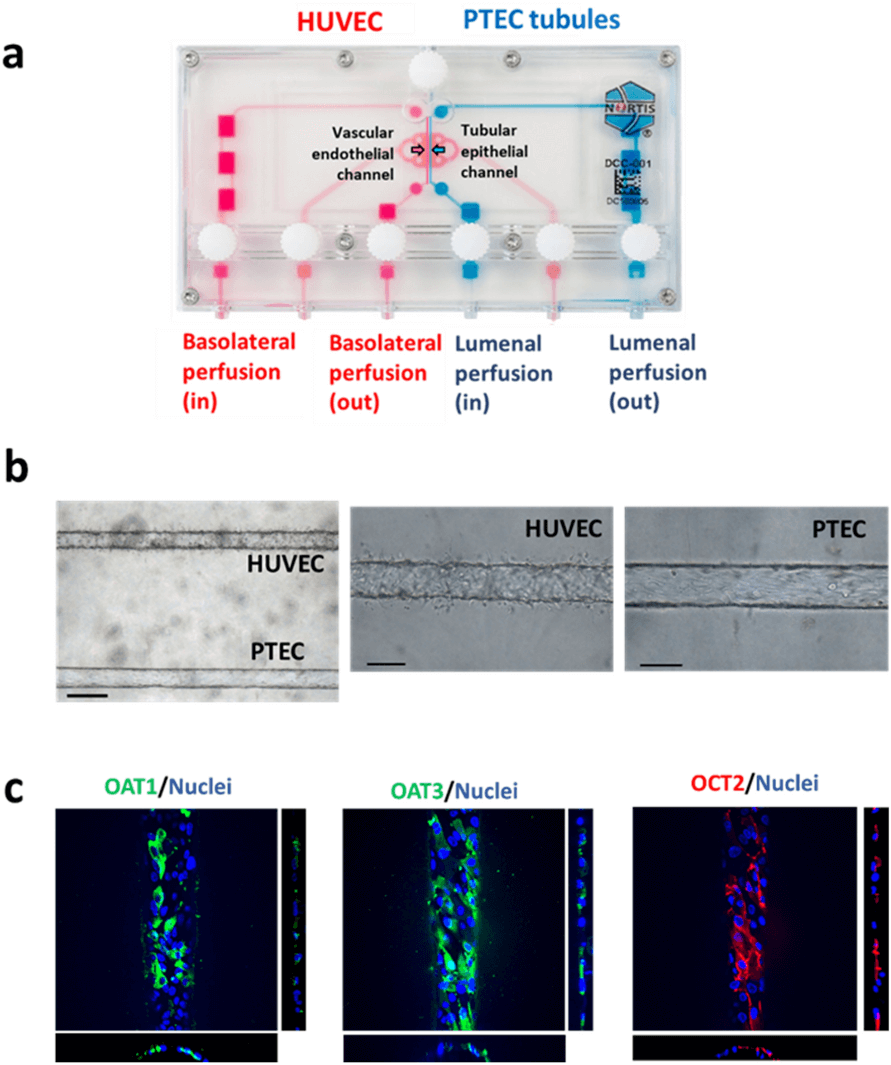 图1. 血管化人近端小管微生理系统的构建。
图1. 血管化人近端小管微生理系统的构建。
为了评估 VPT-MPS 中的分泌转运,在存在和不存在 OAT 和 OCT 抑制剂混合物的情况下,将吗啡和 M6G 注入血管通道。在稳态条件下(输注 6 h 后)计算净清除率。在三个不同供体的 VPT-MPS 中进行了运输实验,显示出均匀、非扰动的介质流动特性。图 2 显示了一个代表性供体的数据。实验发现,吗啡和M6G的外排被转运蛋白抑制剂显著削弱,吗啡的内在清除率平均下降了 74.3%,M6G 的外排平均降低了 63.6%,这表明通过 OATs 和 OCT2 的主动分泌可能有助于吗啡和 M6G 的肾清除。
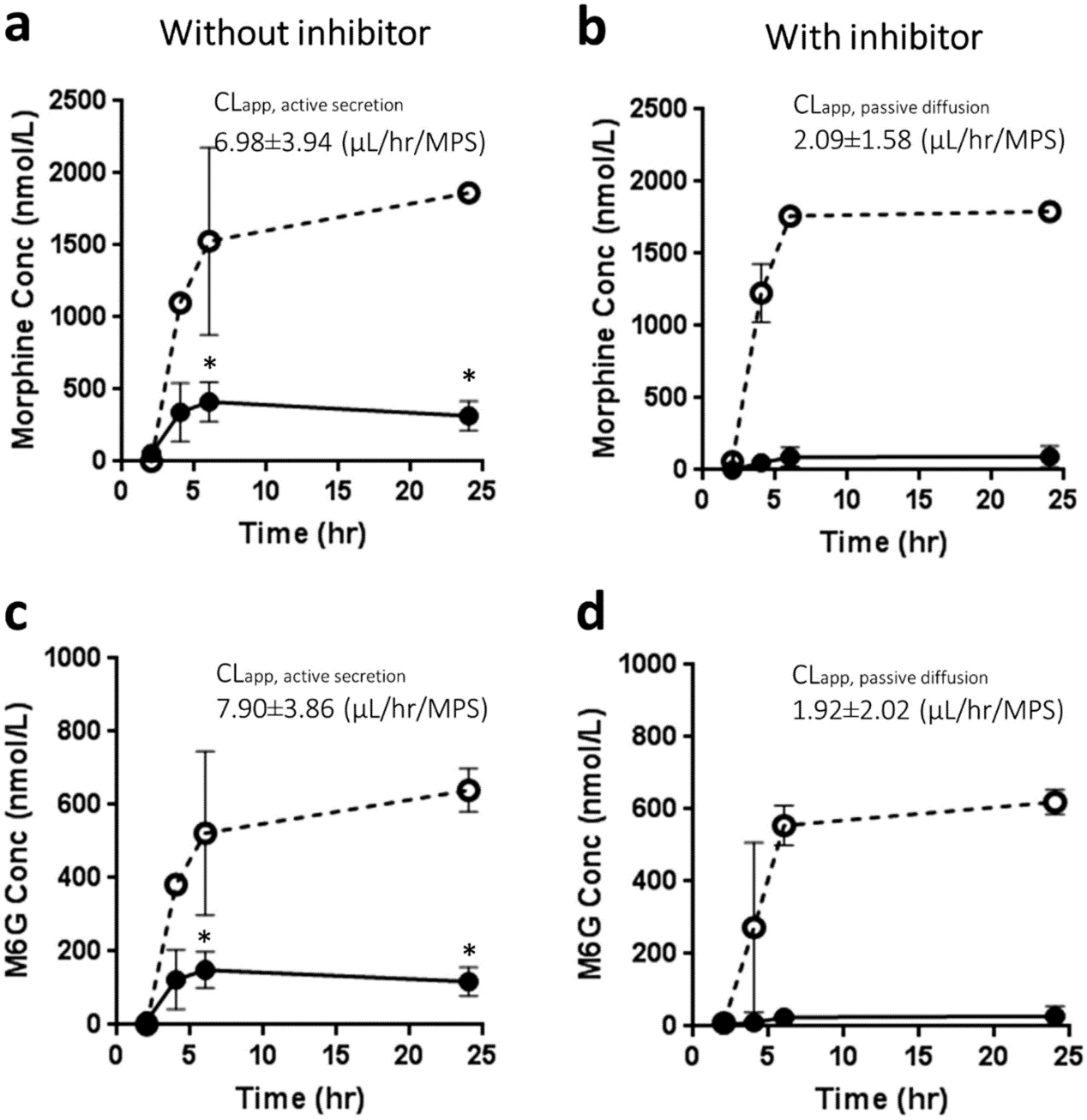 图2. 吗啡和 M6G 通过 VPT-MPS 的运输。
图2. 吗啡和 M6G 通过 VPT-MPS 的运输。
为了测试体外 VPT-MPS 吗啡和 M6G 数据是否可用于模拟人体内吗啡和 M6G 肾脏清除率和血浆浓度-时间曲线,开发了吗啡-M6G 母体-代谢物全身 PBPK 模型,结构如图 3 所示。转运蛋白介导的主动分泌或主动重吸收以黑色虚线箭头显示。双向 pH 依赖性被动扩散以双箭头显示。
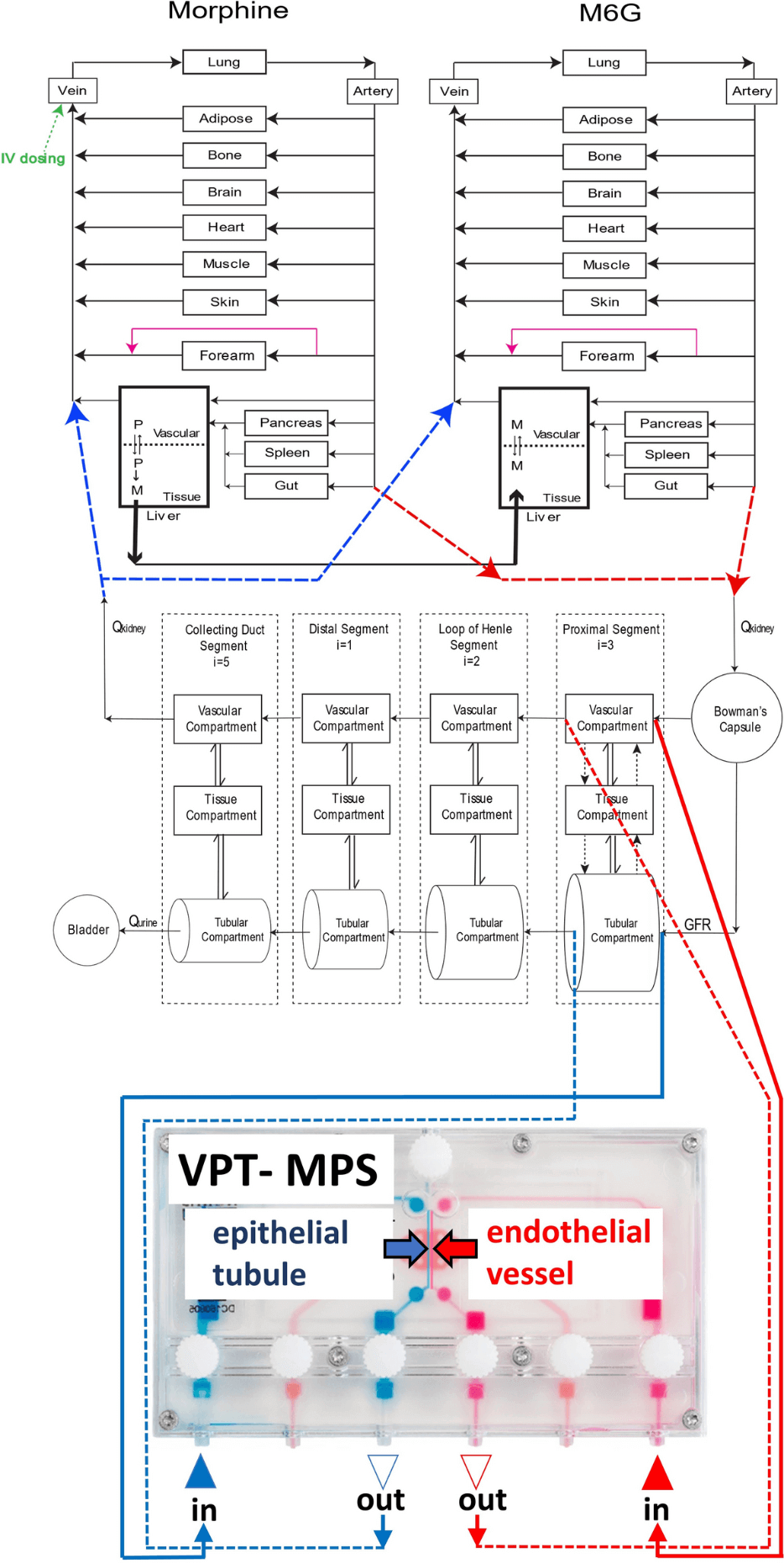 图3. 吗啡-M6G母体-代谢物全身PBPK模型的结构。
图3. 吗啡-M6G母体-代谢物全身PBPK模型的结构。
利用健康受试者静脉注射吗啡或 M6G 后观察到的血浆吗啡和 M6G 浓度时间数据,独立验证了吗啡(图4a和4b)和M6G(图4c和4d)药物模型。然后,利用对健康受试者静脉注射吗啡后观察到的血浆 M6G 浓度-时间数据,验证了吗啡-M6G 母体-代谢物的联系。吗啡和 M6G 模拟的绝对平均倍数误差值从 1.18 到 1.33 不等,都在预先设定的 2 倍模型接受标准之内,表明在健康受试者中,表明模型验证成功,并且对健康受试者的吗啡和 M6G 模型参数具有高置信度。
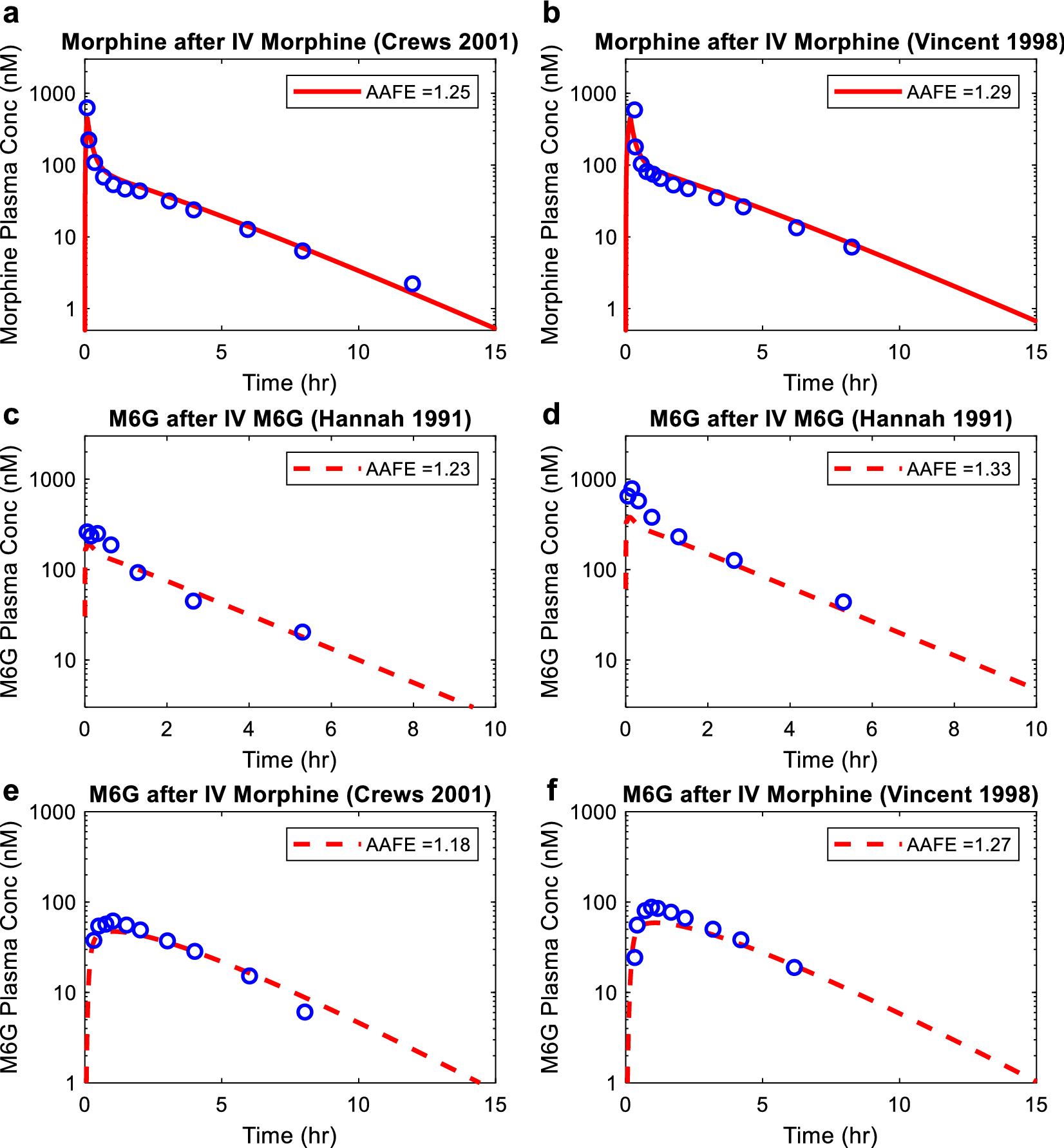 图4. 健康受试者中吗啡和 M6G 血浆浓度-时间曲线的模拟。
图4. 健康受试者中吗啡和 M6G 血浆浓度-时间曲线的模拟。
经模型验证后,该模型被用以研究 CKD 患者中吗啡和 M6G 的分布。首先,模拟了吗啡和 M6G 在 CKD 多个阶段的肾脏清除情况,肾小球滤过率(GFR)估计值范围从 3 mL/min 到 120 mL/min(图5a)。模拟结果显示,在整个 CKD 进展过程中,M6G 肾脏清除率比吗啡肾脏清除率高 10-30%(图5a)。接着,在终末期肾病(end stage kidney disease, ESKD)患者静脉注射吗啡后,使用观察到的血浆吗啡和 M6G 浓度-时间曲线来验证吗啡和 M6G 的 CKD 模型。CKD 模拟的绝对平均倍数误差值范围从 1.22 到 1.30(图5b,5c),均在预先定义的 2 倍模型接受标准内,证明了吗啡和 M6G 从健康受试者到 CKD 患者的成功模型外推。这表明,通过适当的计算机框架,从 VPT-MPS 获得的体外结果可以转化为体内结果。
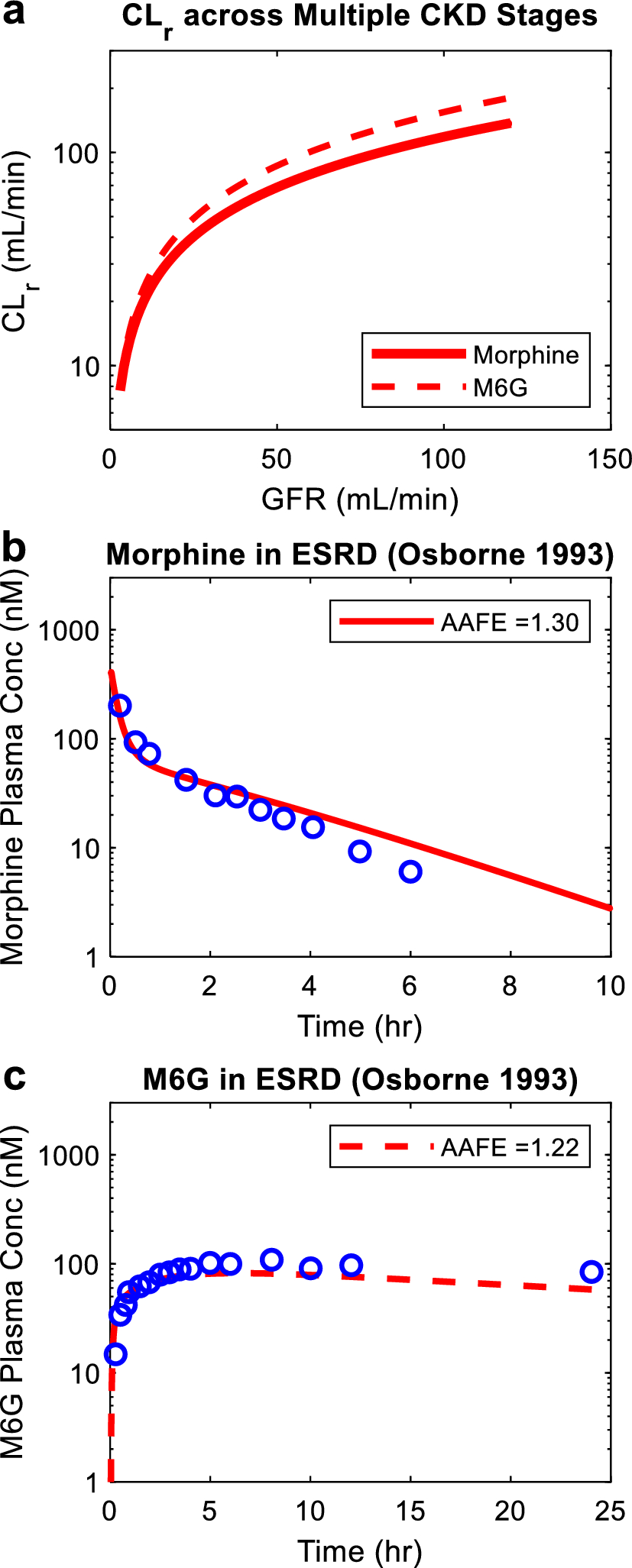 图5. 慢性肾病患者吗啡和 M6G 肾脏清除率和血浆浓度-时间曲线的模拟。
图5. 慢性肾病患者吗啡和 M6G 肾脏清除率和血浆浓度-时间曲线的模拟。
随着 CKD 患者阿片类药物过量和不良事件的增加,越来越需要能够准确预测敏感人群中阿片类药物处置的体外模型,以减轻阿片类药物过量、依赖和成瘾的风险。在该研究中,以 VPT-MPS 与计算机建模方法相结合,生成被动渗透性和主动分泌数据,可以预测健康受试者和肾功能不全患者中吗啡及其活性代谢物 M6G 的分布。验证结果表明,这种方法可以成功地预测健康受试者和 CKD 患者中的肾脏清除率和血浆浓度-时间曲线,绝对平均倍数误差小于 1.5,表明 VPT-MPS 与 PBPK 建模有可能弥合计算机模型和体内之间的差距。此外,这种方法还可以进一步外推到各种药物和研究化合物,以先验了解对患者群体的肾脏和全身性影响。
文献链接:https://www.nature.com/articles/s41598-021-00338-y
作为全球优质的器官芯片模型开发服务供应商,安必奇拥有丰富的体外模型构建、器官芯片开发等代理经验。我们的肾脏器官芯片模型可实现样本滤过、原尿形成和尿素重吸收等功能,具有微环境可控、测量信息丰富、成本低、自动化和高通量等许多优点。此外,目前已整合了全套的器官芯片构建、体外筛选技术一站式服务,致力于为国内外药物开发企业及机构的创新药物评价提供高效的服务和解决方案。欢迎免费咨询!
24小时服务在线

