环境性肠功能障碍(Environmental enteric dysfunction, EED)是一种慢性肠道炎症,与儿童营养不良、生长迟缓、认知障碍和对口服疫苗反应减弱相关,其特点是肠道绒毛变短、肠道屏障功能受损和营养吸收减少。EED 以前被描述为“热带肠病”或“环境肠病”,近年来由于其对中低收入国家数百万儿童的破坏性影响而重新受到关注。由于目前没有成熟的 EED 体外模型,只有受限颇多的动物模型,对该疾病的机理了解有限,使得诊断生物标志物或开发治疗药物等相关研究推进困难。
2022 年 6 月 23 日,来自哈佛大学的研究团队在 Nature Biomedical Engineering 杂志上发表了题为“肠道芯片的营养缺乏概括了与环境肠道功能障碍相关的损伤特征”的研究论文。该研究开发了一种由 EED 患者类器官来源的肠上皮细胞构建的人类肠道芯片模型,并在缺乏烟酰胺和色氨酸的营养缺陷型培养基中培养。基因表达和生理变化测定结果表明,这种体外器官芯片模型与 EED 患者样本中的变化相当。因此,这种 EED 相关肠道损伤的器官芯片模型可能有助于分析该疾病的分子调控、遗传和营养基础,并对候选药物的筛选测试意义重大。

该研究团队之前描述过一种双通道微流控人类肠道芯片,内衬是从患者衍生的类器官中分离出来的人类肠道上皮,当在芯片上培养时,在连续流动和类似蠕动的机械变形下,会发生绒毛分化,积累粘液并表现出体内肠道的许多特征(图 1a)。此外,转录分析表明,当由类器官衍生的十二指肠上皮填充衬里时,这种肠道芯片比用于制造芯片的类器官更接近体内人类十二指肠。为了确定肠上皮对 EED 表型的贡献,研究人员使用从健康或 EED 患者十二指肠的手术活检来源的类器官创建了肠上皮细胞内衬的肠芯片(分别为健康芯片和 EED 芯片)。与健康芯片相比,EED 芯片显示出 287 个基因的差异表达(86 个上调,201 个下调)(图 1b)。
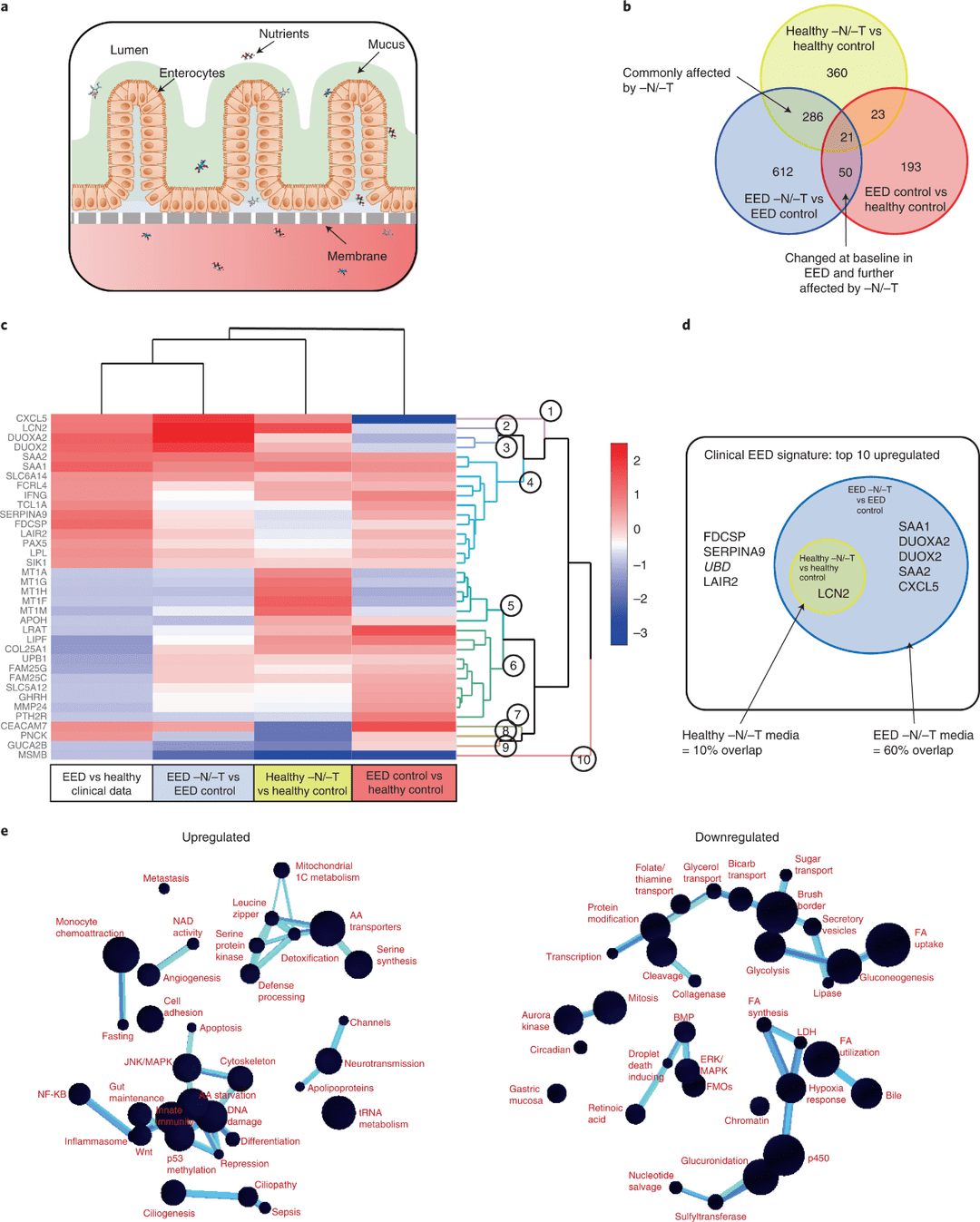 图1. 营养缺乏的 EED 芯片再现了EED患者的转录特征。
图1. 营养缺乏的 EED 芯片再现了EED患者的转录特征。
研究人员将这种差异基因表达谱与临床 EED 特征进行了比较。对照组为接受胃肠道症状调查其内镜和组织学检查结果正常的人。当比较二者在正常培养基(即存在所有营养物质)中培养的基因谱时,差异表达基因与临床 EED 特征有一些重叠,包括较显著的金属硫蛋白(MT1X,MT1A、MT1F、MT1H、MSMB 和 MT1M;基因树状图簇 5)的共同下调(图 1c)。接着,进行了相同的实验,但使用了缺乏烟酰胺和色氨酸(-N/-T)的培养基。比较暴露于营养缺乏的健康芯片(healthy -N/-T 芯片)与健康对照芯片的表达谱时,检测到 690 个基因的差异性表达(556 个上调,124 个下调)(图 1b)。相反,当 EED 芯片暴露于营养缺乏培养基时,观察到与临床 EED 特征更接近的无监督层次结构聚类(EED -N/-T 芯片与 EED 对照芯片)(图 1c)。在 -N/-T 培养基中培养 EED 肠芯片产生了 969 个基因的差异表达(522 个上调,447 个下调)(图 1b)。这表现为抗菌基因(SAA1、SAA2、DUOXA2、DUOX2 和 CXCL5;基因树状图簇 1、3 和 4)的上调,金属硫蛋白以及代谢和消化基因(SLC6A14 和 GUC2AB;基因树状图簇 4 和 9)的下调。这种一致性在临床 EED 特征的前 10 个上调基因中十分明显,其中 6 个在 EED 芯片暴露于营养缺乏的培养基时也被上调(图 1d)。
由于转录组分析显示参与细胞生长和肠道屏障形成的途径下调,进行了微分干涉对比(DIC)和免疫荧光显微镜分析,证实了健康和 EED 肠道芯片在营养缺乏(-N/-T)条件下培养时,与使用完全培养基的对照组相比,绒毛状结构的生长急剧下降(图 2a,2b)。上皮高度的量化显示,去除这些营养物质会导致健康和 EED 芯片中的绒毛明显钝化,与在完全培养基中培养的相同芯片相比,上皮高度分别降低 70% 和 80%(图 2c)。通过实时成像和荧光凝集素染色对粘液积累的分析还表明,当暴露于营养缺乏条件下时,健康芯片和 EED 芯片都表现出更薄的粘液层(图 2d,2e)。此外,肠道屏障功能评估显示,当暴露于营养缺乏条件下时,健康芯片和 EED 芯片都表现出小的但具有统计学意义的降低(图 2f)。
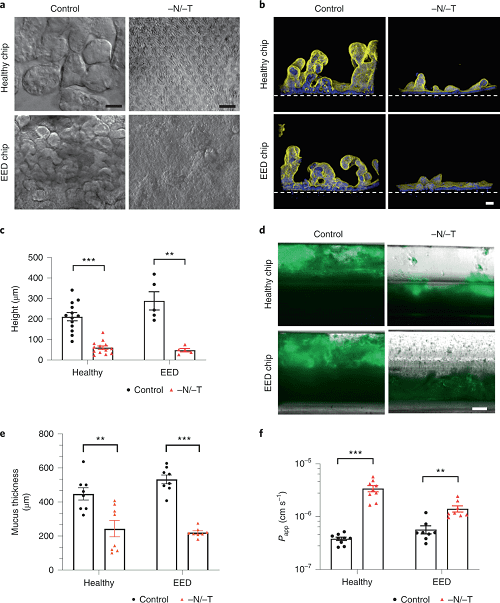 图2. 肠道绒毛萎缩和屏障受损。
图2. 肠道绒毛萎缩和屏障受损。
转录组分析还显示,营养缺乏导致与重要营养成分的吸收和加工有关的多个基因下调,包括脂肪酸、某些氨基酸和碳水化合物(图 1e、3a、4a)。这具有临床意义,因为营养物质的吸收减少是 EED 的另一个标志,它影响到儿童的体重和线性增长以及认知发展。此外,使用荧光标记的十二烷酸对脂肪酸的细胞摄取进行量化,发现与健康和 EED 对照组芯片相比,暴露于营养缺乏的情况下,healthy -N/-T 芯片和 EED -N/-T 芯片对脂肪酸的吸收分别减少了 1.68 倍和 1.69 倍(图 3c)。这些发现与临床数据是一致的,这些数据同样显示患有 EED 的儿童的脂肪酸代谢受损,并表明即使在健康的肠道中,仅营养缺乏也足以减少脂肪酸的吸收。
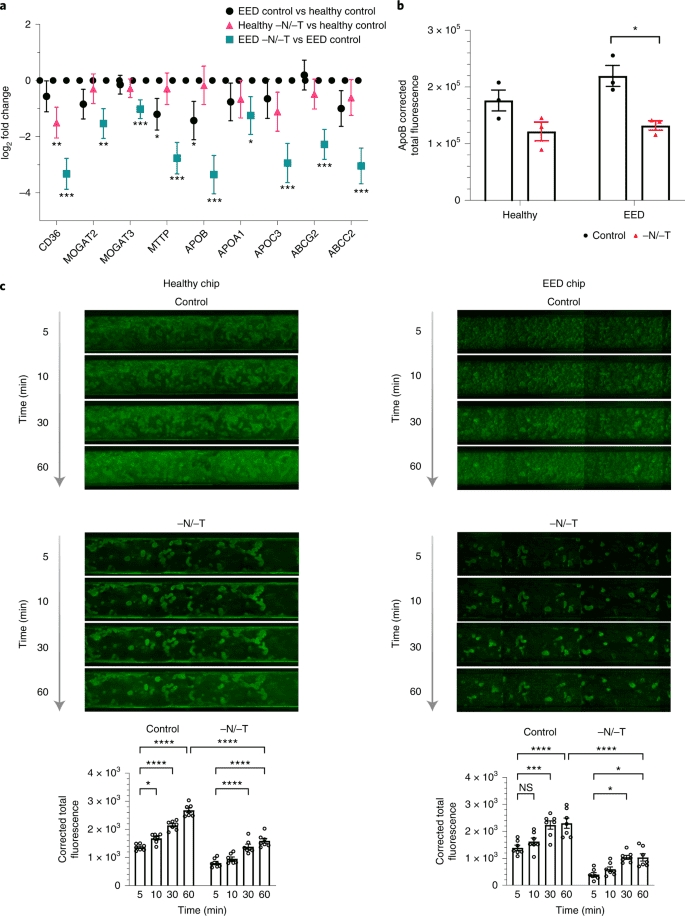 图3. 肠道营养吸收减少。
图3. 肠道营养吸收减少。
在肠道中,膳食蛋白质被分解成短肽和游离氨基酸,这些短肽和游离氨基酸被肠细胞吸收,这些短肽和游离氨基酸是各种器官和组织的组成部分和能量来源。接下来探讨了健康肠芯片和 EED 肠芯片在摄取氨基酸方面的差异。转录组分析显示,EED 对照组芯片与健康对照组芯片相比,吸收和代谢因子被下调,包括溶质载体家族 2(促进葡萄糖转运体)成员 2(SLC2A2)和溶质载体家族 2(促进葡萄糖/果糖转运体)成员 5(SLC2A5)。其他营养转运蛋白(如氨基酸吸收和代谢因子)被发现在 EED 芯片中因 -N/-T 缺乏而反应出明显下调,包括 SLC36A1,其编码质子偶联氨基酸转运蛋白1、负责刷状边缘肽消化的 ANPEP 膜酶丙氨酸肽酶、视黄醇结合蛋白 2(RBP2),细胞色素 P450,27 家族,A 亚家族,和多肽 1(CYP27A1)(图 4a)。
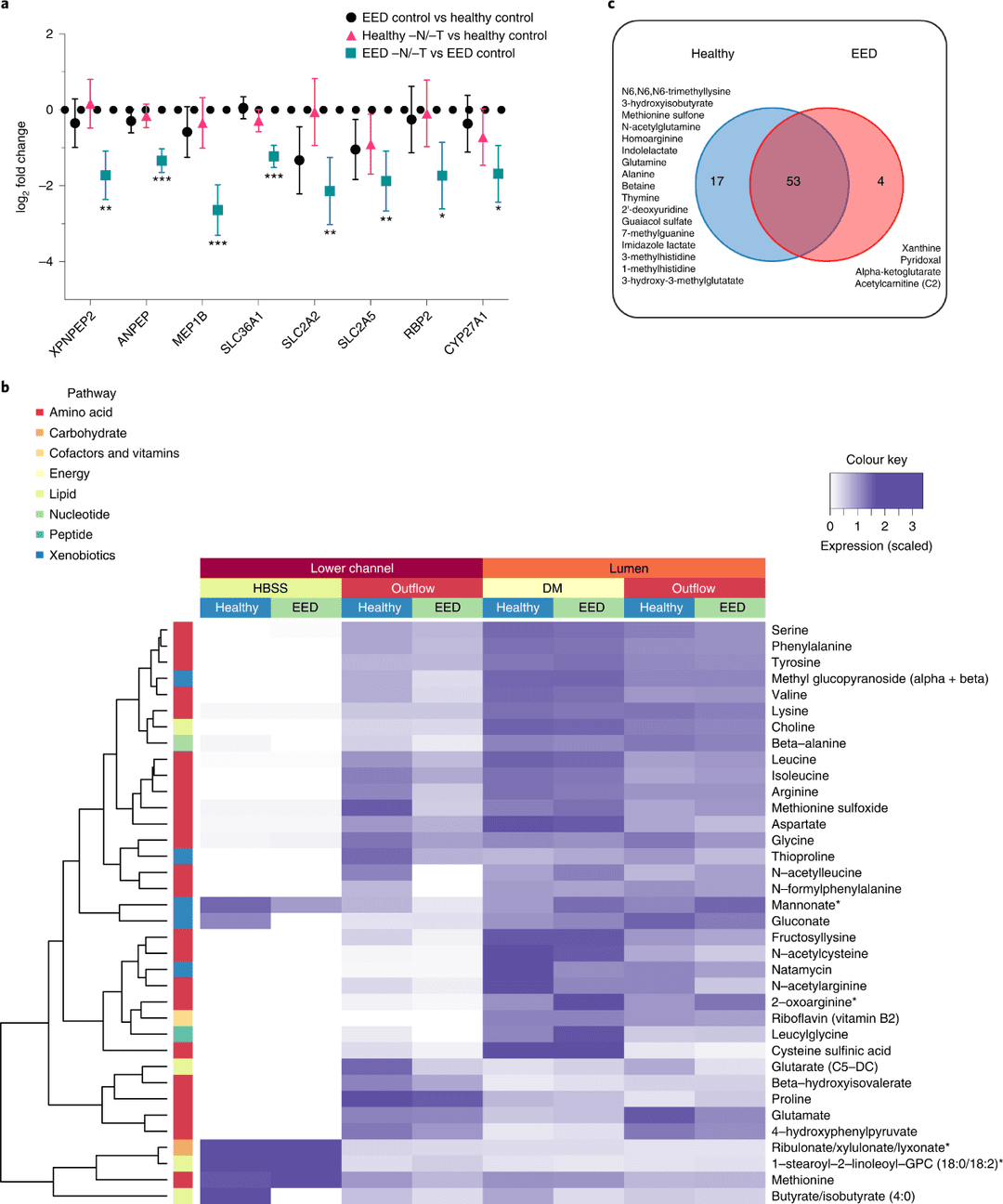 图4. 氨基酸摄取和代谢异常。
图4. 氨基酸摄取和代谢异常。
然后,研究人员通过液相色谱串联质谱(LC-MS/MS)进行非靶向代谢组学分析,评估了健康肠芯片和 EED 肠芯片在对照培养基中生长的营养物质的吸收差异,以分析上皮对营养物质的摄取和这些分子从肠上皮的腔内转移到底层的基底通道的情况。与在对照培养基中生长的健康芯片相比,检测到 EED 肠道芯片 36 种代谢物表现出较低的转运,主要包括氨基酸代谢物,也包括与核苷酸、辅助因子、脂质、碳水化合物和外源性途径相关的代谢物(图 4b)。值得注意的是,这些代谢物中有 9 种是先前确定为在马拉维发育迟缓儿童血清中减少的氨基酸。此外,LC-MS/MS 分析还发现有 74 种代谢物是由肠道细胞分泌的,因为它们在灌注介质中不存在或含量极低(<5%)。其中有 17 种是健康对照芯片所特有的,包括与氨基酸代谢有关的途径的产物、核苷酸、异生物代谢以及脂类等(图 4c)。
肠道炎症改变是 EED 的一个关键组成部分,转录分析显示,当 EED 或健康芯片暴露于营养缺乏培养基时,编码关键炎症标志蛋白如脂联素 2(LCN2)和再生胰岛衍生蛋白 3α(REG3A)的基因会被上调(图 1c)。使用多重 ELISA 测定法量化 9 种关键肠道细胞因子的表达,发现与在控制培养基中培养的相同芯片相比,我们在healthy -N/-T肠道芯片的上皮腔中检测到更高水平的几种细胞因子(IL-6、ICAM、VCAM、IL-33、MCP-1、MIP-1α 和 IL-8)(图 5)。抗菌肽 Reg3A 因这些芯片中的营养缺乏而下调。有趣的是,在完全培养基中生长的 EED 肠芯片显示出所分析的所有分泌细胞因子的水平降低,而当这些芯片在营养缺乏的培养基中生长时,它们的水平显著上升(图 5)。分析下层实质或血管通道中的细胞因子水平时,观察到了类似的反应。然而,炎症细胞因子 IL-8、IP-10 和 MCP-1的 水平显著升高(图 5)。
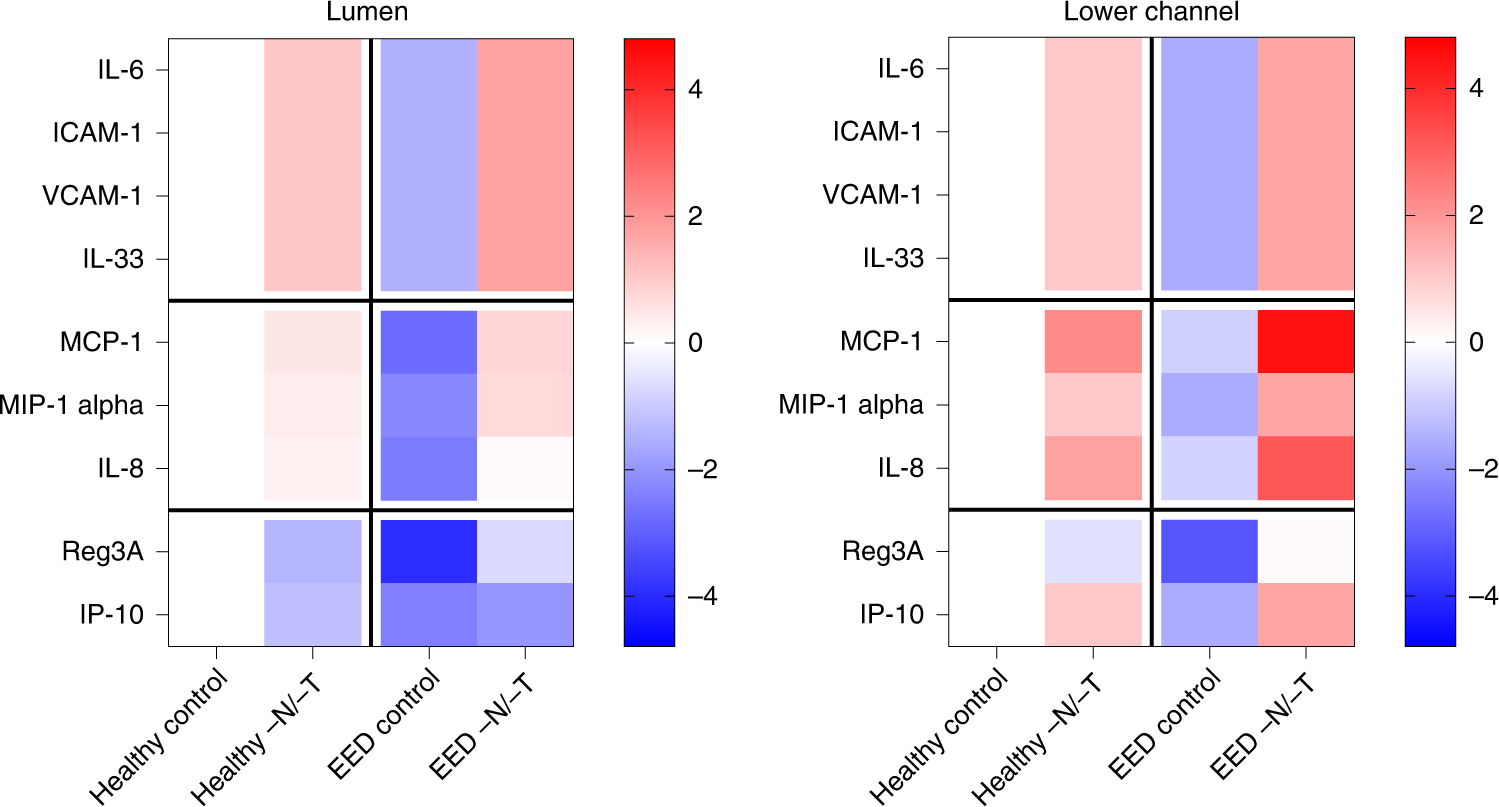 图5. 炎症介质的改变。
图5. 炎症介质的改变。
该研究利用人体肠道芯片技术,利用从 EED 和健康患者肠道活检中获得的细胞创建了体外 EED 模型。与其他先进的体外模型(如肠道类器官)相比,肠道芯片具有独特的优势,其直接进入设备的两个平行流动通道可以对肠道屏障功能以及经上皮的吸收和运输进行定量分析。使用这种方法,在表型和功能水平上探索了营养缺乏对疾病表现的影响。研究结果表明,暴露于营养缺乏培养基下,EED 芯片模拟了 EED 患者转录组的关键特征,包括抗菌基因的上调和金属硫蛋白以及参与消化和代谢的基因的下调。此外,营养缺乏会诱发类似的肠绒毛萎缩,屏障功能破坏,以及氨基酸和脂肪酸吸收的变化。因此,使用该模型能够将这些不同的反应具体归因于营养缺乏、肠道上皮的遗传或表观遗传变化,或两者的结合,而这些区别在临床研究中是不可能做到的。通过整合免疫细胞成分、个性化定制等方向的创新,这种体外 EED 模型可能有助于进一步了解这种疾病的病理生理学以及开发更具针对性的治疗方法。
原文链接:https://www.nature.com/articles/s41551-022-00899-x
作为全球高品质临床前药物开发服务供应商,安必奇生物拥有丰富的体外模型构建、器官芯片开发等代理经验。提供优良、完善的器官芯片设计及开发服务,以帮助客户获取高仿、节能的生理学研究及药物开发工具。目前已建立能够模拟心脏、肝脏、肺、肾、脑、肠等器官的微结构和功能的芯片模型。可从材料、制备技术、仪器、以及商业化等方面实现个性化定制。欢迎免费咨询!
24小时服务在线

